



《电解质的电离》离子反应PPT课件
第一部分内容:素养目标
1.通过实验,以变化的思想领会电离的概念,从而掌握电解质概念的内涵和外延,逐步提升科学探究与创新能力。
2.通过对电解质和电离概念的认识,能从宏观和微观相结合的视角重新认识酸、碱、盐的概念。
3.通过归纳总结,学会用电离方程式表示某些酸、碱、盐的电离,培养证据推理与模型认知意识。
... ... ...
电解质的电离PPT,第二部分内容:课前篇自主预习
知识铺垫
1.导电性实验证明:NaCl、NaOH、H2SO4的水溶液能够导电,蔗糖、酒精的水溶液不导电。
2.常见的酸有HCl、H2SO4、HNO3(写化学式),常见的碱有NaOH、KOH、Ba(OH)2和Ca(OH)2。
3.NaCl、Na2SO4等属于正盐,而NaHSO4属于酸式盐。
新知预习
一、电解质
1.定义
在水溶液里或熔融状态下能够导电的化合物。如HCl、H2SO4、NaOH、Ca(OH)2、NaCl、KNO3等。
温馨提示在水溶液里和熔融状态下都不能导电的化合物,叫非电解质。如蔗糖、酒精等。
2.电解质溶液或熔融电解质导电的原因(以NaCl为例)
(1)电解质导电必须具备的条件:有自由移动的离子。
(2)NaCl属于电解质,固体中含有带电微粒Na+、Cl-,但这些离子不能自由移动,故氯化钠固体不导电。
(3)NaCl固体溶于水时,在水分子的作用下,Na+、Cl-进入水中,形成了能够自由移动的带电粒子,故NaCl溶液可导电。
(4)氯化钠固体受热熔化时,离子的运动随温度升高而加快,克服了离子间的相互作用,产生了能够自由移动的Na+和Cl-,故熔融NaCl也能导电。
【微思考1】(1)NaCl溶液能导电,NaCl溶液是电解质吗?
(2)纯H2SO4在熔融状态时不导电,H2SO4不是电解质吗?
提示(1)NaCl溶液是混合物,不是电解质。
(2)H2SO4在水溶液中能导电,所以H2SO4是电解质。
二、电解质的电离
1.定义
电解质溶于水或受热熔化时,形成自由移动的离子的过程。
2.表示方法——电离方程式
(1)酸的电离(如H2SO4):H2SO4 2H++SO_4^2"-" 。
(2)碱的电离(如NaOH):NaOH Na++OH-。
(3)盐的电离(如CuSO4):CuSO4 Cu2++SO_4^2"-" 。
3.从电离的角度认识酸、碱、盐:
(1)酸:电离时生成的阳离子全部是氢离子(H+)的化合物;
(2)碱:电离时生成的阴离子全部是氢氧根离子(OH-)的化合物;
(3)盐:由金属阳离子或铵根离子(N )与酸根阴离子组成的化合物。
自主测试
1.判断正误(正确的打“√”,错误的打“×”)。
(1)在水溶液里和熔融状态下都能导电的化合物是电解质。 ( )
(2)在水中能导电的化合物一定是电解质。 ( )
(3)电解质发生电离需要通电才能进行。 ( )
(4)电解质是化合物,电解质溶液是混合物。 ( )
(5)溶于水能电离产生H+的电解质一定属于酸。 ( )
(6)氯化钠晶体不能导电,是由于其中不含离子。 ( )
答案(1)× (2)× (3)× (4)√ (5)× (6)×
2.现有以下物质:①氮气 ②液态CO2 ③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔化的KNO3 ⑨NaOH溶液
请回答下列问题(填序号):
(1)以上物质能导电的是__________。
(2)以上物质中属于电解质的是__________。
(3)③⑧两种物质的电离方程式为
③__________,
⑧__________。
答案(1)④⑧⑨ (2)③⑤⑧ (3)③HCl=H++Cl- ⑧
... ... ...
电解质的电离PPT,第三部分内容:课堂篇探究学习
电解质及其导电性
问题探究
(1)上图所示装置为试验物质导电性装置,在干燥的烧杯中依次分别加入下列物质,观察灯泡是否变亮?加入烧杯中的物质是否是电解质?
(2)通过以上实验,讨论:电解质本身是否一定导电?电解质导电的环境一般是什么环境?
(3)如果将无水酒精或酒精水溶液放入上面的烧杯中,灯泡都不亮,则酒精是否属于电解质?
深化拓展
电解质的判断
(1)从物质分类看:电解质与非电解质都属于化合物。单质、混合物既不是电解质,也不是非电解质。
常见的酸(常见强酸HCl、H2SO4、HNO3、HI、HBr、HClO4等;常见弱酸H2CO3、H2S、H2SO3、CH3COOH等)、碱[常见强碱NaOH、KOH、Ca(OH)2、Ba(OH)2等;常见弱碱NH3·H2O、Fe(OH)3、Cu(OH)2等]、盐、多数金属氧化物、水都是电解质,而多数非金属氧化物、多数有机物、NH3等属于非电解质。
(2)从物质性质看:电解质在一定条件下导电。电解质导电的条件是电解质溶于水或熔融状态,二者具备其一即可。有些电解质溶于水导电,但熔融状态下不导电,如HCl气体;有些电解质只在熔融状态下才能导电,如BaSO4。
(3)某化合物是不是电解质与其溶解性无关。如蔗糖能溶于水,但蔗糖是非电解质;难溶于水的盐,如BaSO4、CaCO3是电解质。
(4)溶于水能导电的化合物不一定是电解质。如CO2水溶液能导电,但不是CO2分子本身电离产生离子,而是它与水反应生成的H2CO3电离出自由移动的离子,所以H2CO3是电解质,CO2不是电解质。
素能应用
典例1下列说法正确的是( )
A.液态氯化氢不能导电,但氯化氢是电解质
B.Cu和Cl2的水溶液都能导电,所以说Cu和Cl2都是电解质
C.某化合物的水溶液可以导电,该化合物一定是电解质
D.BaSO4难溶于水,所以说BaSO4不是电解质
答案A
解析A项,HCl的水溶液能够导电,所以说HCl是电解质;B项,Cu和Cl2都是单质,不属于电解质;C项,CO2的水溶液能导电,但CO2不是电解质;D项,BaSO4虽然难溶,但溶解的部分全部电离,且BaSO4在熔融状态下能导电,所以BaSO4是电解质。
易错提醒电解质电离的条件有两种:在水溶液里或熔融状态,并不需要通电;电离是电解质导电的前提条件。
变式训练1电解质不仅在工农业生产中占有重要地位,而且在各种生命活动中也起着重要作用。下列有关电解质的叙述正确的是( )
A.化合物都是电解质
B.纯水的导电性很差,但水也是电解质
C.电解质在水中一定能导电,在水中导电的化合物一定是电解质
D.NaNO3固体不导电,所以NaNO3不是电解质
答案B
解析在水溶液里或熔融状态下能够导电的化合物属于电解质,A项错误;水是电解质,B项正确;电解质导电是有条件的,电解质在水中不一定能导电,如硫酸钡,在水中导电的化合物也不一定是电解质,如二氧化碳,C项错误;NaNO3溶液能导电,所以NaNO3是电解质,D项错误。
... ... ...
电解质的电离PPT,第四部分内容:随堂检测
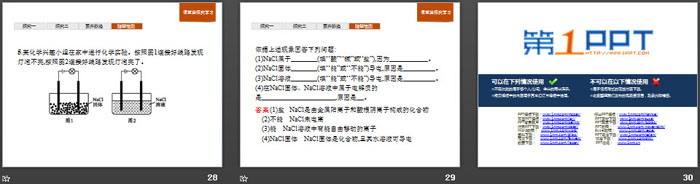
1.电解质是指在水溶液里或熔融状态下能够导电的化合物。几位同学对此定义中的关键词发表了以下理解或看法,你认为不正确的是( )
A.“或”字意味着水溶液里、熔融状态下这两个条件只需具备其中之一就行
B.“能够导电”是指该物质本身能够电离出离子而导电,而不是它发生反应后的生成物电离出离子而导电
C.“化合物”指明了该物质不能是单质,更不能是混合物
D.像硫酸钡这样难溶的化合物就不可能是电解质了
答案D
解析D项错误,硫酸钡在熔融状态下可以导电,属于电解质。
2.下列说法正确的是( )
A.石墨有较好的导电性,所以石墨属于电解质
B.由实验可知NH3的水溶液具有一定的导电性,所以NH3是电解质
C.液态HCl、固态NaCl均不能导电,所以HCl、NaCl均不是电解质
D.蔗糖在水溶液里和熔融状态下均不能导电,所以蔗糖不是电解质
答案D
解析石墨是单质,不是化合物,因此不属于电解质,A项不正确;NH3的水溶液能导电,是因为NH3与H2O反应生成NH3·H2O,NH3·H2O电离产生自由移动的离子而导电,B项不正确;虽然液态HCl、固态NaCl不导电,但它们的水溶液均能导电,故两者均属于电解质,C项不正确。
... ... ...
关键词:人教版高中化学必修一PPT课件免费下载,电解质的电离PPT下载,离子反应PPT下载,.PPT格式;
更多关于《 离子反应 电解质的电离 》PPT课件, 请点击 离子反应ppt电解质的电离ppt标签。
《电解质的电离 离子反应》元素与物质世界PPT课件(第2课时离子反应):
《电解质的电离 离子反应》元素与物质世界PPT课件(第2课时离子反应) 第一部分内容:素养目标 1.通过实验和实验事实理解离子反应的实质;以变化的思想领会离子反应发生的条件及其应用,..
《电解质的电离 离子反应》元素与物质世界PPT课件(第1课时电解质的电离):
《电解质的电离 离子反应》元素与物质世界PPT课件(第1课时电解质的电离) 第一部分内容:素养目标 1.通过实验,以变化的思想领会电离的定义,从而掌握电解质定义的内涵和外延,逐步提升科..
《电解质的电离 离子反应》元素与物质世界PPT(第2课时离子反应):
《电解质的电离 离子反应》元素与物质世界PPT(第2课时离子反应) 第一部分内容:学习目标 课程标准 1.通过实验事实认识离子反应。 2.认识并掌握离子反应发生的条件。 3.掌握离子方程..






